
Stato dell’arte nel trattamento dei gliomi cerebrali
Le Possibilità della Chirurgia
Vincenzo Esposito
Professore Ordinario di Neurochirurgia,”Sapienza” Università di Roma
La chirurgia dei gliomi presenta importanti problemi legati alle modalità di sviluppo e crescita di questi tumori . I più importanti sono costituiti da:
• Crescita intracerebrale con infiltrazione di parenchima normale. Questi tumori nascono e si sviluppano all’interno del tessuto cerebrale, infiltrando progressivamente tessuto cerebrale normale. Non è quindi possibile asportarli radicalmente senza coinvolgere tessuto normale.
• Localizzazione in aree profonde. Quando questi tumori crescono in regioni profonde del cervello, non sono direttamente visibili dalla superficie cerebrale esposta dopo l’apertura del cranio e della dura madre. Sono necessari dei sistemi di guida per raggiungerli con precisione. Il tragitto chirurgico va studiato con attenzione, per evitare per quanto possibile di attraversare regioni cerebrali integre, con possibili danni funzionali a queste ultime.
• Localizzazione in aree funzionalmente critiche. La rimozione di tumori cerebrali localizzati all’interno di regioni cerebrali con funzioni importanti per la vita di relazione (ad esempio le funzioni motorie e il linguaggio) può comportare un danno serio e irreversibile. L’adozione di sistemi di monitoraggio di queste funzioni è in grado di ridurre significativamente questo rischio


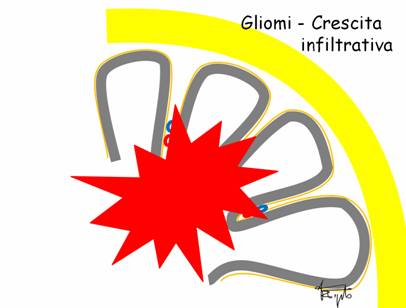
Modalità di crescita dei gliomi
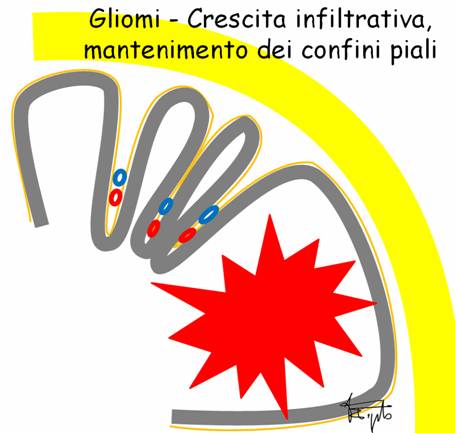
I gliomi crescono all’interno del cervello, infiltrando progressivamente tessuto sano. Quando l’epicentro della crescita è nella profondità della sostanza bianca, vengono rapidamente interessate strutture con funzioni importanti, come i nuclei della base ed i fasci di sostanza bianca (vie piramidali, vie associative del linguaggio). La rimozione radicale risulta impossibile in questi casi: l’unica possibilità è praticare una biopsia cerebrale (vedi). In molte situazioni tuttavia la crescita neoplastica avviene più in superficie, nella sostanza bianca delle circonvoluzioni. Inizialmente, il glioma si accresce espandendo il volume della circonvoluzione di origine, mentre i confini piali verso le circonvoluzioni vicine sono mantenuti: in questo contesto la chirurgia radicale è possibile, purché non siano direttamente coinvolte aree funzionalmente critiche. Quando il glioma, nel proseguire la sua crescita, raggiunge la sostanza bianca profonda, la modalità di crescita diviene identica a quella del primo caso e la rimozione radicale non è più possibile.

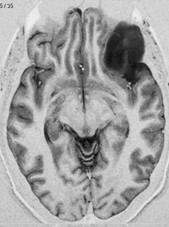
Biopsia cerebrale
La biopsia è un intervento chirurgico effettuato allo scopo di ottenere la diagnosi istologica di una lesione cerebrale, in casi in cui l’intervento di asportazione comporti rischi elevati o non sia indicato. Può essere praticata con diverse tecniche (con metodica stereotassica, in neuronavigazione o a cielo aperto). Nel porre indicazione alla biopsia, bisogna tenere presente che l’intervento non è esente da rischi. La sensibilità diagnostica varia, essendo maggiore nei pazienti immunocompetenti (82- 99%), rispetto agli immunodepressi (56-96%). E’ inoltre significativamente maggiore nelle lesioni che si potenziano dopo somministrazione di mezzo di contrasto (99% vs 80%). Le complicazioni consistono essenzialmente nel rischio emorragico, sensibilmente più alto nei pazienti immunodeficienti (1-12%, versus 1-4% nei pazienti immunocompetenti). La mortalità è compresa fra lo 0,5 e l’1%.
Chirurgia ablativa dei gliomi cerebrali
In molti casi, come già detto, è possibile una chirurgia ablativa con intento di radicalità.
Utilità della microchirurgia. L’uso del microscopio operatorio è importante. In microchirurgia l’aspetto dei gliomi, alterato rispetto al tessuto sano, è più facilmente riconoscibile: il tessuto cerebrale sano è distinguibile per la chiara e netta distinzione fra sostanza grigia e bianca, che non è presente nel tessuto tumorale. Inoltre è possibile visualizzare particolari di anatomia chirurgica difficilmente riconoscibili ad occhio nudo, come la presenza delle lamine di pia madre, che segnano in molti casi i confini di queste neoplasie, oppure l’aspetto tipicamente striato dei nuclei della base, che segnano il limite profondo delle neoplasie coinvolgenti l’insula. Inoltre la microchirurgia è fondamentale per aprire i corridoi chirurgici costituiti da scissure e solchi, che consentono l’accesso a zone profonde del cervello. L’apertura microchirurgica della scissura silviana permette ad esempio l’esposizione dell’insula, struttura ricoperta dai lobi frontale e temporale, evitando il passaggio attraverso parenchima cerebrale sano. Impiegando la microchirurgia, è molto meno richiesta la retrazione rigida del cervello con spatole, in quanto l’illuminazione è più efficace e le varie angolazioni possibili con il microscopio operatorio consentono di visualizzare adeguatamente la zona di interesse senza dislocare il cervello. La microchirurgia offre infine maggiori possibilità di risparmiare strutture vascolari sane, cui questi tumori possono aderire, limitando la morbidità vascolare.
Altre note tecniche. La differente consistenza dei gliomi è un segno importante chirurgicamente e consente in molti casi di delimitare precisamente la neoplasia dal tessuto sano. In molti casi è utile l’impiego della neuronavigazione, allo scopo di localizzare neoplasie profonde e di meglio delinearne i limiti.
Zone funzionali
Poiché le neoplasie cerebrali possono sorgere in vicinanza o all’interno di regioni cerebrali dotate di funzioni importanti per la vita di relazione, quali linguaggio e movimenti, è fondamentale poter monitorare queste funzioni. Esistono vari maniere di realizzare questo compito:
1) Chirurgia da sveglio (“awake surgery”)
Poiché la superficie cerebrale è insensibile, è possibile operare in anestesia locale. Il paziente è sveglio durante l’intervento, e questo consente di valutare direttamente l’effetto della stimolazione della corteccia cerebrale (mapping corticale) o delle fibre di sostanza bianca (mapping subcorticale) su varie funzioni, identificando le regioni che non debbono essere danneggiate ai fini della preservazione delle funzioni stesse. Inoltre l’andamento di tali funzioni viene valutato di continuo durante la fase di rimozione chirurgica (monitoraggio). L’awake surgery tuttavia ha alcuni svantaggi: non tutte le persone sono adatte psicologicamente a sopportare un intervento da svegli (si pensi ad esempio ai bambini); se l’intervento dura a lungo è possibile che il paziente, con l’andar del tempo, collabori sempre meno e verso il termine dell’intervento le sue risposte siano progressivamente meno affidabili; la stimolazione cerebrale può provocare crisi epilettiche, e può rendersi necessario sedare il paziente in sala operatoria, con il risultato che questi non è più valutabile per un certo periodo di tempo e tutta l’equipe chirurgica è forzata ad attendere il risveglio del paziente per proseguire la valutazione e l’intervento. Nonostante questi svantaggi, l’awake surgery è la tecnica più usata nel mondo per la chirurgia in aree critiche.
2) Alternative alla awake surgery
Il mappaggio e monitoraggio delle aree motorie può essere effettuato in anestesia generale, stimolando elettricamente la corteccia cerebrale e registrando segnali elettromiografici sull’ emisoma contro laterale all’emisfero cerebrale interessato. Bisogna utilizzare tecniche anestesiologiche idonee, con farmaci che non deprimano l’attività neurofisiologica cerebrale ed elettromiografica: non si usano anestetici volatili, ma sol farmaci endovenosi (TIVA, Totally Intravenous Anesthesia), e il paziente non è curarizzato. Al fine di non deprimere i segnali neurofisiologici, è altresì importante operare in normotensione e che la temperatura corporea sia normale. Per evitare il rischio di crisi comiziali intraoperatorie, si pratica all’induzione una infusione endovenosa di difenilidantoina, che ha il vantaggio di essere immediatamente efficace senza deprimere l’attività cerebrale. Con tale tecnica è possibile eseguire un brain mapping corticale o sottocorticale. Inoltre si può monitorare continuamente lo stato funzionale della via piramidale, stimolando periodicamente, una volta al secondo, l’area motoria primaria tramite una strip di elettrodi posizionata sulla corteccia rolandica: la registrazione elettromiografia consente di ottenere i potenziali evocati motori (Motor Evoked Potentials, MEP). La tecnica dei MEP è estremamente vantaggiosa, in quanto controlla continuamente, durante la rimozione chirurgica, l’integrità funzionale di tutta la via piramidale, sia della corteccia che delle fibre: inoltre verifica anche l’efficienza della sua vascolarizzazione. I MEP, in caso di diminuzione o abolizione, forniscono al chirurgo in tempo reale l’avviso che qualcosa non va, consentendo di adottare immediatamente le opportune contromisure: interruzione delle manovre chirurgiche, aumento della pressione arteriosa media ed irrorazione del campo con papaverina. Nella maggior parte dei casi queste manovre consentono il ripristino dei MEP. I MEP sono molto affidabili: i pazienti con MEP immodificati al termine dell’intervento si risvegliano sicuramente senza deficit motori, i pazienti con MEP assenti si risvegliano con un deficit motorio, ed i pazienti con MEP transitoriamente alterati possono risvegliarsi con un deficit motorio reversibile.
Per la valutazione del linguaggio, che richiede ovviamente la piena collaborazione del paziente, vengono invece impiantati con un intervento di craniotomia in anestesia generale degli elettrodi subdurali che coprono la superficie cerebrale interessata. Il giorno successivo il paziente, tornato in reparto, viene sottoposto ad una sessione di stimolazione della superficie corticale mentre esegue dei test per la valutazione del linguaggio. Localizzate le aree corticali funzionali, il giorno dopo il paziente viene riportato in sala operatoria, ed in anestesia generale si procede alla rimozione delle neoplasia preservando le aree funzionali. Questa tecnica ha il vantaggio di poter essere impiegata anche in pazienti psicologicamente inadatti alla awake surgery, come i bambini, in quanto la valutazione del linguaggio avviene al di fuori della sala operatoria, mentre le fasi chirurgiche vere e proprie avvengono in anestesia generale. Essendo il paziente in una condizione psicologica molto più favorevole che in sala operatoria, i test di valutazione possono essere più complessi e condotti per un periodo di tempo maggiore. L’eventuale verificarsi di una crisi epilettica può essere gestito in maniera più semplice, in quanto il paziente non è a cranio aperto in sala operatoria. Poiché gli elettrodi subdurali, una volta aperta la dura, possono essere facilmente fatti scivolare al di sotto dei margini dell’apertura del cranio, non è necessario praticare ampie craniotomie per valutare estese porzioni di corteccia, ma è sufficiente esporre la sola neoplasia. Fra gli svantaggi, il più ovvio è quello che sono richiesti 2 successivi interventi chirurgici: tuttavia, poiché il secondo intervento avviene a breve distanza dal primo, la riapertura è molto rapida, e la somma totale dei tempi richiesti dai due interventi è inferiore a quella di una singola awake surgery, in quanto tutta la fase di valutazione avviene al di fuori della sala operatoria. Tale tecnica è inoltre limitata alla valutazione della corteccia,mentre non è possibile il mappaggio sottocorticale. Infine essa richiede personale ed attrezzature dedicate (stanze per monitoraggio Video-Elettroencefalografico), di solito disponibile solo nei centri che praticano routinariamente chirurgia dell’epilessia.
Conclusioni
• Le attuali tecnologie e tecniche chirurgiche rendono possibile la resezione radicale di un gran numero di gliomi cerebrali, sia di basso che di alto grado, con morbidità molto contenuta.
• La biopsia cerebrale è attualmente confinata ad un ridotto numero di casi.
• La sopravvivenza e la qualità della vita sono in miglioramento continuo.
Per la corrispondenza:
gpcantore@neuromed.it